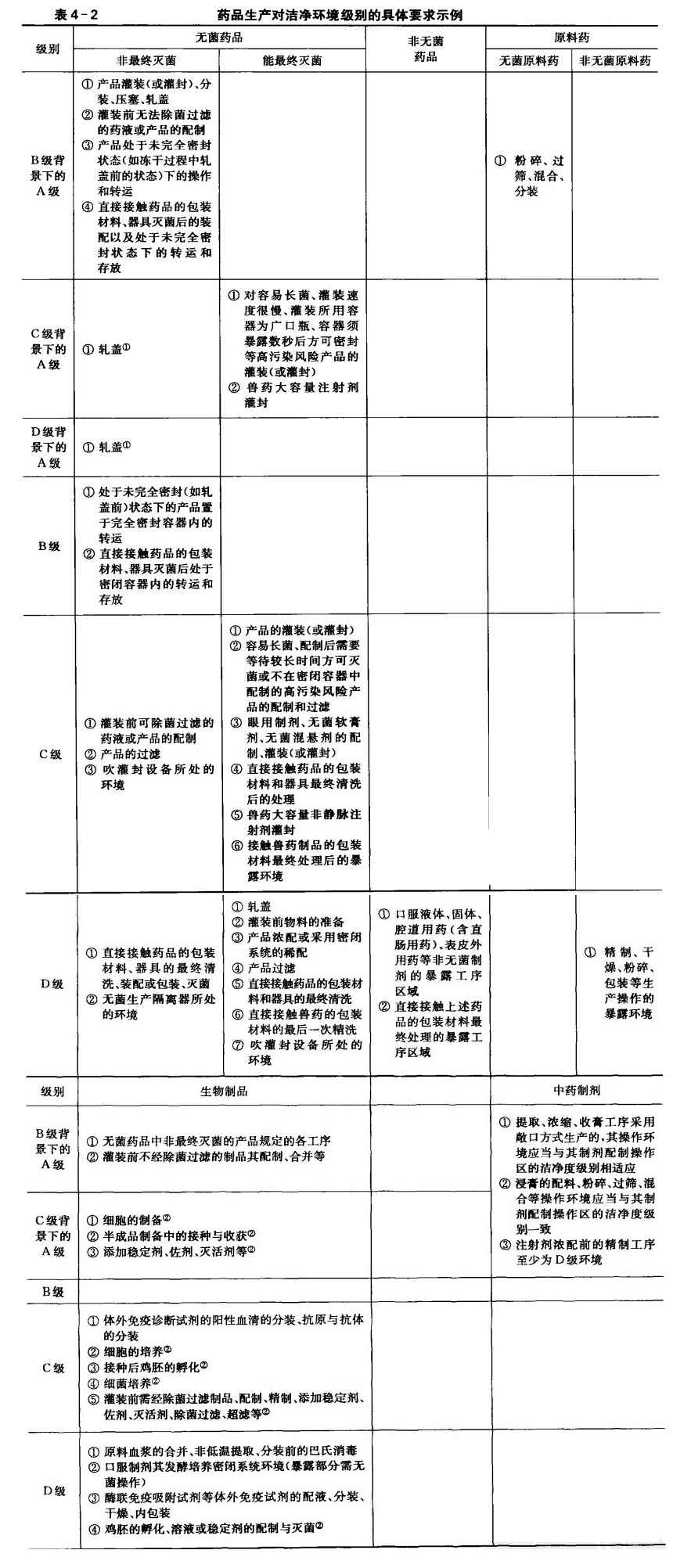
本文主要对制药各工序或各药种制订的具体空气洁净度级别。由于制订的级别比较集中明确,具有很好的操作性,这一点和国外GMP相比是一大特色。
现接GMP(2010)和兽药GMP(2002),将有洁净度要求的药品品种和相关工序整理成表4-2。 按GMP定义,表中的无菌药品是指法定的药品标准中列有无菌检查项目的制剂和原料药,包括:眼用制剂、无菌软膏剂、无菌混悬剂等。
表中的非无菌药品则是药品标准中未列无菌检查项目的制剂和非无菌原料药及无菌原料生产中非无菌生产工序操作的药品。
根据GMP的要求,在确定一个制药车间设计级别时,首先应明确是哪一类药,其次要知道是什么剂型,再次是能否最终灭菌,需要无菌检查否?还要知道容量的大小,过滤的有无,工序暴露与否,只有完全回答清楚这些问题,才能准确给级别定位。最后还应有节约的原则,根据工艺和生产量,能用局部5级就不用全室5级,能用较小面积的局部5级就不用大面积的局部5级。当然面积不能小而不适用,美于这一点可见第7章针剂一节。
关于生物制品还须指出,各类制品生产过程中如涉及高危致病因子,其空气净化系统除要满足表4 2中规定的级别外,还应符合特殊的要求下隔离、封闭或生物安全等